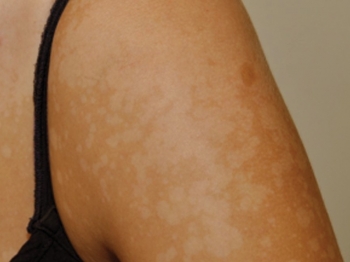
 Красный плоский лишай (КПЛ) - единственное распространённое кожное заболевание поражающее кожу, слизистые оболочки, волосы и ногти.
Красный плоский лишай (КПЛ) - единственное распространённое кожное заболевание поражающее кожу, слизистые оболочки, волосы и ногти.⠀Не заразен.
⠀2/3 случаев встречаются у пациентов 30-60 лет. Страдают оба пола. Всего около 1% населения.
⠀Поражение слизистой оболочки встречается у 60-70% взрослых пациентов. У детей реже, примерно в 1/3 случаев. Волосы и ногти у детей страдают очень редко.
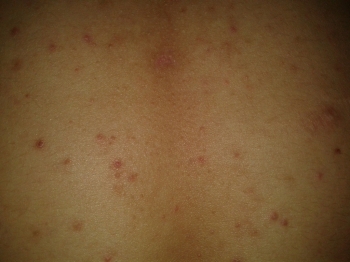 Если вас беспокоят прыщи на спине, а также на плечах или груди, грамотные лечение, уход за кожей и ряд бытовых мер помогут вам вернуть чистую кожу.
Если вас беспокоят прыщи на спине, а также на плечах или груди, грамотные лечение, уход за кожей и ряд бытовых мер помогут вам вернуть чистую кожу.И иногда вы можете добиться этого даже самостоятельно. Но расчитывать на то, что вы сможете справиться своими силами, применяя рекомендации из списка ниже можно только если вас беспокоят комедоны: «чёрные и белые точки», неровности, немногочисленные воспалённые элементы; заболевание дебютировало недавно.
Если же у вас много глубоких, болезненных высыпаний – лучше не откладывать посещение врача и обсудить с ним, какие из 12 советов будет целесообразно оставить на фоне назначенной врачом терапии.
⠀Советы по уходу и образу жизни:
1. Ежедневная обработка кожи спины и других страдающих областей тела средством для умывания с содержанием бензоила пероксида – пену необходимо оставлять на коже на 2-5 минут до качественного смывания.
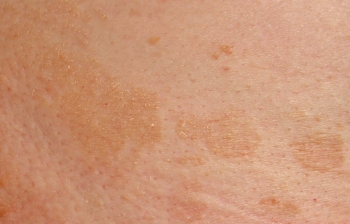 Розовый лишай - острое кожное заболевание с саморазрешающимися высыпаниями. В целом, в определении сказано всё, что нужно знать пациенту.
Розовый лишай - острое кожное заболевание с саморазрешающимися высыпаниями. В целом, в определении сказано всё, что нужно знать пациенту.⠀Для окружающих стоит добавить - абсолютно не заразное.
⠀«Острое» - то есть не хроническое, болеть годами не будете, переболели и забыли.«Саморазрешающимися» - то есть само пройдёт, можно не лечить.
И оба эти факта, безусловно, радуют заболевших. Расстраивает, как правило, длительность болезни: от 4 до 10 недель (и всё это время лечить не надо).
⠀В чем причина? Нет, ни посещение бассейна, ни питание, ни заболевания желудка/кишечника/печени, ни контакт с больным человеком или незнакомым животным не являются причинами розового лишая. Болеют чаще подростки и молодые люди.
 Существует два варианта отшелушивания себорейных чешуек, которые можно применять самостоятельно.
Существует два варианта отшелушивания себорейных чешуек, которые можно применять самостоятельно.1. Вариант бытовой и недорогой: тёплое растительное масло нанести на кожу головы на 30 минут, затем расчесать волосы детской мягкой щёточкой в разные стороны (не жёсткой расчёской) и качественно смыть масло привычным средством для мытья головы.
Этот способ не рекомендуется хотя бы до 6 месяцев жизни малыша (чем позже, тем лучше). Почему?
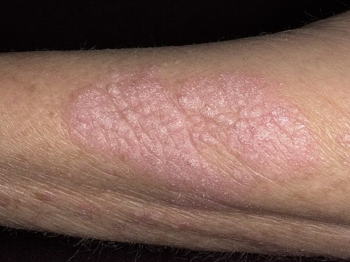
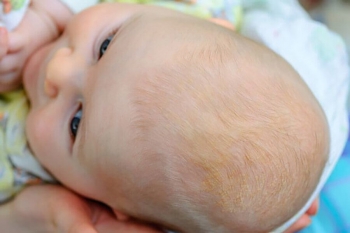 Себорейный дерматит - распространённое заболевание.
Себорейный дерматит - распространённое заболевание.⠀Различают детскую и взрослую формы. И младенческая форма себорейного дерматита не является фактором риска развития его во взрослом возрасте.
⠀Шелушащиеся (чешуйки часто жёлтые), иногда мокнущие покраснения возникают у малышей на участках богатых сальными железами. На голове, лице, груди, в складках - проявления себореи.
⠀У маленьких детей сложность представляет дифференциальный диагноз с атопическим дерматитом. Общих черт у заболеваний имеется несколько, так что некоторые авторы даже причисляют младенческую форму себорейного дерматита к особой, лёгкой форме атопического. Но различить патологии всё же возможно.
 Важны не только действия, но и отношение.Здесь и о том, и о другом для здоровья и красоты вашей кожи.
Важны не только действия, но и отношение.Здесь и о том, и о другом для здоровья и красоты вашей кожи.1️⃣ Признайте её самостоятельность.
Относитесь к ней, как к отдельному прекрасному и сложноустроенному органу , а не как к исключительно «зеркалу организма», «оболочке» или элементарной плёночке, которая не позволяет нам рассыпаться на горстку костей и органов в луже жидкостей.
⠀
2️⃣ Принимайте её такой, какая она есть.
Даже, если она болеет, если происходит что-то, что не нравится вам. Только приняв то, что ваша кожа страдает псориазом/экземой/акне/розацеа или другими заболеваниями или здорова, но легко краснеет на солнце/активно вырабатывает кожное сало/склонна к сухости и шелушению и т.д. вы сможете начать полноценно лечиться от дерматологических заболеваний или решать косметические задачи.
⠀
3️⃣ Запаситесь терпением.
Не стоит ждать результатов от лекарств, процедур или косметики на следующий же день. У кожи и её придатков свои темпы обновления и внутренних процессов - и они не спешат.
 Кратко и по делу: чего не должно быть в вашей жизни, если вы боретесь с угревой болезнью.
Кратко и по делу: чего не должно быть в вашей жизни, если вы боретесь с угревой болезнью.Сохраняйте и применяйте.
1. Выдавливание/расцарапывание элементов. Кроме того,что останутся рубцы и пятна постакне ничего вы этим самостоятельно не добьетесь.
2. Скрабы. Про них была отдельная статья на сайте. Точно нет , ни здоровым, ни страдающим акне.
3. Средства для ухода за кожей из массмаркета (популярные магазины косметики). Это возможно только после консультации с вашим дерматологом.
4. Частая смена средств для ухода за кожей и применение нескольких продуктов сразу (любимая пенка, разрекламированный лосьон, привычный крем, новый тоник, многообещающая маска, опять лосьон, запасной крем и ещё точечный стик - и всё за один день...)
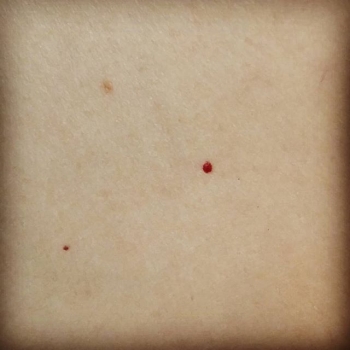
Красные точки от 1 до 10 мм диаметром существующие на коже давно или появляющиеся новые - это гемангиомы.
⠀Абсолютно безопасные разрастания внутреннего слоя сосудов кожи, которые спонтанно и по пока необъяснимым причинам появляются тем чаще, чем чем старше мы становимся. Удаление, например, электрохирургическим методом или лазером возможно. Но по исключительно эстетическим соображениям и личному желанию.
⠀Выделяют отдельный тип гемангиом - младенческие.
Чтобы достичь значительных успехов в борьбе с заболеванием этот список идеально сопоставить с 10 «нет» при акне, которые также опубликованы на сайте.
⠀Что абсолютно можно и даже нужно пациентам, страдающим акне?
1️⃣ Качественный ежедневный уход за кожей с применением аптечной/профессиональной косметики. Здорово, если вам подходят средства одной фирмы и гаммы, но это не принципиально. Важно подобрать оптимальные именно для вашей кожи текстуры и составы. Пусть даже комплект сложится от разных производителей.
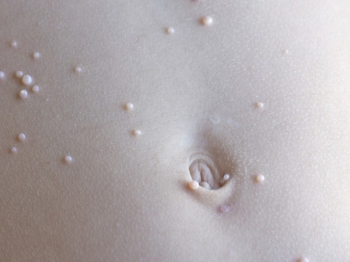
Это Вирусное заболевание. Дети болеют чаще. Этот факт определяется посещением детских коллективов.
⠀ Заражение происходит при контакте кожа-к-коже или через предметы (общее полотенце и т.п.) Интересно, что подобное может являться и причиной самозаражения - распространения элементов на другие области тела при соприкосновении с высыпаниями.
⠀Появляются маленькие узелки цвета кожи с углублением в центре.