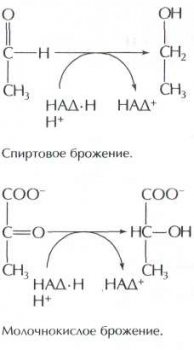
Во многих анаэробах молочная кислота — конечный продукт превращения глюкозы. И она же является той органической молекулой, которая в конце концов принимает на себя электроны. Поэтому получение молочной кислоты из глюкозы называется молочнокислым брожением. Клетки анаэробов выделяют её в окружающую среду как шлак При большой физической нагрузке молочная кислота образуется в условиях недостатка кислорода и у высших организмов. Это происходит в клетках мышечных тканей. Молочная кислота должна удаляться из них с кровью, иначе наступает переутомление мышц. Позднее в печени молочная кислота вновь превращается в глюкозу.
Как мы помним, реакции, связанные с переводом энергии в АТФ, представляют собой реакции окисления. В клетке есть специальная молекула, которая
играет по отношению к электронам ту же роль, что АТФ по отношению к энергии. В одних реакциях она принимает электроны, в других — отдаёт. Имя клеточного аккумулятора электронов — никотинамидадениндинуклеотид, сокращённо — НАД.
Гликолиз протекает таким образом, что НАД сначала принимает электроны, а затем его восстановленная форма, которую обозначают НАД•Н, снова окисляется. При восстановлении одной молекулы НАД до НАД•Н выделяется энергия, достаточная для образования высокоэнергетической связи в одной молекуле 1,3-дифосфоглицериновой кислоты (та самая энергия, которая потом запасается в виде АТФ). На каждую молекулу глюкозы приходится две молекулы НАД•Н. Обратное окисление НАД•Н в НАД происходит на последней стадии гликолиза. В результате этой реакции из пировиноградной кислоты образуется молочная кислота.
Молекула НАД состоит из двух нуклеотидов. Один из них содержит основание аденин, присутствующее в нуклеотидах ДНК, а другой — положительно заряженное соединение никотинамид, который и определяет способность НАД быть аккумулятором электронов. Никотинамид может приобретать два электрона в некоторых окислительно-восстановительных реакциях, которые протекают в организме. Условно можно представить, что НАД реагирует с двумя атомами водорода. Каждый такой атом имеет по одному электрону. Один атом водорода никотинамид забирает к себе полностью, а другой отпускает, предварительно отобрав у него электрон. В итоге никотинамид получает два электрона:
НАД++2Н®НАД•Н+Н+.
На самом деле, НАД, конечно же, вступает в реакцию не с атомами водорода. Вот как, например, протекает реакция окисления альдегидной группы до карбоксильной:
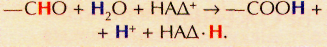
Клетка запасает энергию в АТФ с помощью катаболических реакций, в основном это реакции окисления. Попавшие в клетку пищевые молекулы отдают электроны специальным веществам, которые тоже в свою очередь окисляются. Эстафетная передача электронов, безусловно, не бесконечна. У многих организмов, в том числе и у человека, электроны в конце концов достаются молекуле кислорода. Кислород попадает в наш организм из воздуха через лёгкие. Смысл дыхания как раз и состоит в окислении органических молекул кислородом. В результате дыхания химическая энергия запасается в молекуле АТФ. Живые существа, использующие кислород для извлечения энергии, называются аэробами (от греч. «аэр» — «воздух»).
Некоторые организмы, например дрожжи, могут обходиться без кислорода. Есть и такие, для которых кислород просто ядовит. Они получили название анаэробы. К ним относятся некоторые виды бактерий и низших беспозвоночных. Чтобы спрятаться от кислорода, они обитают глубоко в почве, низших слоях водоёмов или в морском иле. Тем не менее энергию анаэробы всё же получают: обогащение энергией в отсутствие кислорода называется брожением. В этом случае электроны достаются не кислороду, а органической молекуле. Большинство учёных считают, что жизнь появилась на Земле ещё в те времена, когда её атмосфера была лишена кислорода. Поэтому, скорее всего, брожение возникло раньше, чем дыхание. Это исторически первый способ извлечения энергии живыми организмами.
Некоторые организмы используют энергию АТФ для выделения света. В клетках таких организмов протекают реакции, в результате которых химическая энергия превращается в энергию света. Чаше всего это происходит у насекомых. Например, светлячки светятся в брачный период. Существуют глубоководные рыбы, которые приманивают с помощью света добычу.
Свечение живых организмов называется биолюминесценцией (от греч. «биос» — «жизнь» и лат. lumen — «свет»), за это отвечает фермент люцифераза (от лат. lux — «свет» и fero — «несу»).
Большое количество запасённой энергии клетка расходует на производство новых химических веществ, необходимых для развития организма, В противовес катаболическим такие реакции учёные назвали анаболическими (от греч. «анаболе» — «подъём»). Поэтому лекарства, стимулирующие рост мыши, называют анаболиками. Их принимают люди, перенёсшие тяжелые травмы и операции. Вместе катаболические и анаболические реакции называются метаболическими (от греч. «метаболе» — «перемена»).
В живой клетке идёт непрерывный процесс в неё поступают одни и выводятся наружу другие химические вещества. Она получает необходимые соединения благодаря питанию. Молекулы, попадающие в организм с пищей, — это полимерные соединения: белки, жиры и углеводы. С ними происходит множество химических превращений, в результате которых крупные молекулы разлагаются до молекул-карликов типа СО2 и воды. В живых организмах действует множество ферментов, управляющих реакциями разложения — катаболическими реакциями (от греч. «катаболе» — «сбрасывание», «разрушение»). Разрушая белки, жиры и углеводы, клетка высвобождает энергию, заключённую в их химических связях. Чтобы использовать эту энергию, клетка предварительно должна её накопить. Для этого необходим своего рода аккумулятор, который имеется в любом живом организме. Такую функцию несёт особое вещество — аденозинтрифосфорная кислота (АТФ).
Эволюция не могла обойти своим вниманием такой важный момент, как выбор постоянного и мощного источника энергии для живых организмов. Наша главная «станция энергоснабжения» — Солнце. Хотя астрономы и называют его звездой-карликом, Земля получает от Солнца около 2•1017 Вт (Дж/с).Этой мощности пока вполне хватает, чтобы обеспечить всё разнообразие жизни.
Зелёные растения, синезелёные водоросли, а также некоторые бактерии могут непосредственно улавливать солнечную энергию. За это их называют фототрофами (от греч. «фотос» — «свет» и «трофе» — «пища»), что переводится буквально как «питающиеся светом». Все другие живые существа, в том числе и человек, не могут напрямую усваивать энергию солнечного света. Их источник -химическая энергия, поэтому такие организмы называются хемотрофами. Однако, по существу, они тоже питаются энергией Солнца. И в этом нет никакого противоречия. Ведь фототрофы переводят солнечную энергию
в химическую, синтезируя при этом разнообразные органические вещества. В результате энергия запасается в химических связях. Травоядные животные питаются растениями, и энергия Солнца попадает к ним уже в химической форме. А плотоядные животные получают энергию, поедая травоядных. Получается, что растительный мир — это «энергетический кормилец» животного мира.
На этикетке самого обычного пакета молока кроме сведений о предприятии-изготовителе, условиях хранения и сроке годности есть и ещё кое-что, на первый взгляд, совершенно не нужное покупателю:
«В 100 г продукта содержится жира — 2,5 г белка — 2,9 г углеводов — 3,9 г Энергетическая ценность 53 ккал».
На самом же деле это очень важная информация. Ведь главное свойство человеческого, как и любого живого, организма — способность извлекать из окружающей среды и запасать энергию.
В активных группах многих ферментов присутствует ион металла, комплексно связанный с органическим веществом. С 1945 г. советские учёные начали исследовать каталитическое действие ионов металлов в разном окружении. Ион Fe3+, содержащийся в каталазе, может и без белкового окружения, в виде обычной соли железа, разлагать пероксид водорода в водном растворе. Вот только каталитическая активность свободных ионов железа в миллиарды раз меньше, чем у фермента. Разлагают Н2О2 и ионы Cu2+. Но когда ионы меди образуют комплекс с молекулами аммиака, их активность возрастает в миллион раз. А если вместо аммиака взять органические амины, то разложение пероксида идёт ещё быстрее.
Сегодня большой ассортимент недорогих ферментов, в том числе высокой чистоты, находит применение более чем в 25 отраслях промышленности, и прежде всего — в лёгкой и пищевой.
Чтобы тесто было пышным, нужен разрыхлитель — углекислый газ. Он выделяется при действии дрожжей на углевод мальтозу. А откуда берётся мальтоза? Она постепенно образуется из крахмала под влиянием амилазы, содержащейся в муке. Обычно собственной амилазы муки недостаточно, и этот фермент добавляют. Протеазы, действующие на клейковину муки, используют, чтобы придать тесту консистенцию, необходимую для удержания углекислого газа. Ведь если он пройдёт сквозь тесто и улетучится, тесто снова опадёт. Добавление ферментов улучшает аромат и вкус хлеба, даёт румяную корку.
И производству алкогольных напитков никак не обойтись без ферментов, содержащихся в дрожжах. Дрожжи с различными ферментными комплексами позволяют получать разные сорта пива. А чтобы напиток не мутнел, в него добавляют протеазы (папаин, пепсин) — они разлагают белковые осадки.
Производство молочных продуктов также немыслимо без ферментов. Простоквашу делают с помощью ферментов молочнокислых бактерий, которые превращают молочный сахар лактозу в молочную кислоту. Для производства кефира берут определённую смесь молочнокислых бактерий и дрожжей, при этом часть содержащейся в молоке лактозы переходит в молочную кислоту, а часть — в спирт. Одновременно идёт также частичный гидролиз белков, поэтому кефир легче усваивается организмом, чем молоко.
Итак, ферментный препарат в виде раствора получен. Он готов к работе, но возникает вопрос: реакция пройдёт, а что дальше? Как отделить фермент от продуктов?
Промышленные каталитические процессы предпочитают вести на твёрдых катализаторах, тогда проблема разделения исчезает. В качестве эксперимента попробовали и фермент прикрепить к твёрдому носителю. Одним из способов такого прикрепления является адсорбция — обратимое связывание вещества с поверхностью твёрдого тела без химического изменения. В 1916 г. впервые было обнаружено, что при адсорбции инвертазы — фермента, расщепляющего сахарозу на более простые углеводы (глюкозу и фруктозу), на угле или гидроксиде алюминия она сохраняет каталитическую активность. А в 1939 г. получен первый патент на применение протеаз, адсорбированных на древесных опилках, для обработки шкур животных.