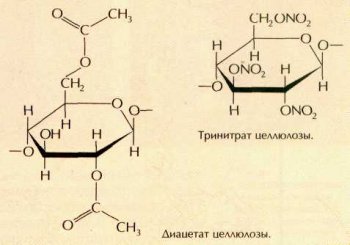
Подобно другим веществам, содержащим гидроксильные группы, целлюлоза вступает в реакцию этерификации с органическими и неорганическими кислотами с образованием сложных эфиров. При этом связи между отдельными фрагментами соединения не разрываются, и возникает полимер, включающий сложно-эфирные группы —COOR—. При взаимодействии целлюлозы с уксусной кислотой или её производными (например, уксусным ангидридом) образуются ацетаты целлюлозы, у которых в каждом звене макромолекулы на эфирные остатки замещены одна, две или три гидроксильные группы.
Ацетаты целлюлозы используются в производстве синтетических волокон (ацетатного волокна).
При нитровании целлюлозы смесью дымящей азотной и концентрированной серной кислот образуется тринитрат целлюлозы, который применяют для приготовления бездымного пороха (пироксилина).
Динитрат целлюлозы служит основным компонентом целлулоида — пластмассы, из которой делают некоторые типы искусственных стёкол.
Бумага (от персидск. «бомбака» — «хлопок») представляет собой материал, состоящий из тонко переплетённых между собой волокон целлюлозы. Отдельные волокна связаны друг с другом посредством водородных связей, которые возникают между гидроксильными группами.
Бумага была изобретена в конце II в. до н. э. в Китае, где её получали из волокон хлопка и бамбука. В VIII в. н. э. секрет изготовления бумаги стал известен арабам, а в IX в. его переняли византийцы.
В Средние века для изготовления бумаги использовали хлопок, пеньку, а также старое тряпьё — хлопковые и льняные ткани. На специальных мельницах их превращали в порошок, который размешивали в воде для получения густой однородной массы. Лишь в XVIII в. было обнаружено, что удобным исходным веществом для производства бумаги может служить древесина. А первые заводы по переработке древесины в целлюлозу появились только в XIX столетии.
Сахар, который вы кладёте в чашку чая или кофе, скорее всего, из сахарной свёклы. Но он мог быть выработан и из сладкого сока других растений. Во многих странах этот продукт получают из сахарного тростника. Хотя с химической точки зрения свекловичный сахар и тростниковый — одно и то же вещество, у них всё же есть отличия. Обнаружить их можно лишь с помощью чувствительного прибора, позволяющего определять соотношение изотопов углерода в образце. В природе углерод встречается в виде двух стабильных изотопов — 12С и 13С, содержание которых, соответственно, 98,892 и 1,108%.
Различие в массах изотопов углерода достаточно велико — около 8 %, и это сказывается на скоростях некоторых химических реакций, идущих в живых организмах. Например, при фотосинтезе растения, поглощая из воздуха углекислый газ, отдают предпочтение более лёгкому изотопу 12С, поэтому во всех живых организмах и продуктах их разложения (угле, торфе, нефти) содержание тяжёлого изотопа 13С немного понижено, тогда как в углекислом газе и карбонатах морского происхождения (известняк из раковин) — повышено.