Простейший представитель класса фенолов — соединение, давшее название всему классу, С6Н5ОН. Это бесцветное кристаллическое вещество (tплав=41 °С) с характерным запахом, плохо растворимое в холодной воде. Попав на кожу, фенол вызывает ожоги, поэтому обращаться с ним нужно осторожно.
Источник фенола — каменноугольная смола, из которой он был впервые выделен в 1834 г. В наше время его получают из бензола и пропилена — кумольным способом, разработанным в 1949 г. советским химиком Рудольфом Юрьевичем Удрисом.
По химическим свойствам фенол отличается от спиртов и бензола. Это слабая кислота, и долгое время его называли карболовой кислотой. Фенол обладает бактерицидным действием — он убивает даже самые стойкие бактерии и микроскопические грибки. Поэтому его водный 5-процентный раствор широко применяли для дезинфекции помещений.
В отличие от бензола, фенол легко окисляется кислородом. При хранении на воздухе его бесцветные кристаллы становятся сначала розовыми, а затем малиново-красными из-за процессов окисления, идущих с образованием свободных радикалов:
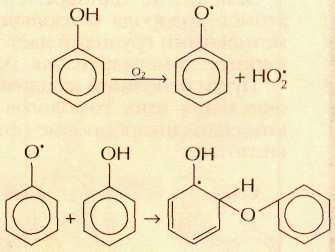
Результатом такого взаимодействия являются ярко окрашенные полифенолы. На этом свойстве основано использование фенола в качестве антиокислителя (его добавляют в некоторые краски, например в гуашь, что придаёт ей характерный запах).
Фенол легко бромируется. Так, при действии бромной воды выпадает белый осадок 2,4,6-трибромфенола. Другой качественной реакцией на фенол является его взаимодействие с хлоридом железа(III), приводящее к возникновению фиолетового окрашивания.
Висмутовая соль 2,4,6-трибромфенола в медицине называется ксероформом. Ещё в XIX столетии это вещество использовали как бактерицидное. Оно входит в состав антисептической мази Вишневского, которая применяется и по сей день как наружное средство при лечении нарывов.
При обработке фенола смесью концентрированных серной и азотной кислот образуются жёлтые кристаллы 2,4,6-тринитрофенола — пикриновой кислоты.
Своим названием она обязана очень горькому вкусу (от греч. «пикрос» — горький). Пикриновая кислота — ярко-жёлтое кристаллическое вещество. В XIX в. она широко использовалась в качестве красителя для шерсти, шёлка, кожи. Впоследствии были обнаружены взрывчатые свойства пикриновой кислоты. Во время Первой мировой войны ею вместе с тротилом начиняли артиллерийские снаряды; правда, вскоре от этого пришлось отказаться. Дело в том, что в отличие от фенола это достаточно сильная кислота, и при её взаимодействии со стальной оболочкой снаряда образуется очень чувствительная к детонации соль — пикрат железа (C6H2(NO2)3O)2Fe. Длительное хранение таких боеприпасов приводит к непредсказуемым взрывам. Однако высокая взрывчатость пикратов всё же нашла своё применение — пикрат свинца (C6H2(NO2)3O)2Pb и по сей день используют в детонаторах взрывных устройств.
При хлорировании фенола образуется пентахлорфенол С6Сl5ОН, производное которого пентахлорфенолят натрия C6Cl5ONa
применяется в качестве средства для консервации древесины. Пропитанная раствором этого вещества, древесина не только не подвержена гниению, но и не горит.
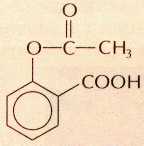
При сплавлении фенола со щёлочью в автоклавах в атмосфере углекислого газа и последующей обработке сплава неорганической кислотой образуются бесцветные кристаллы 2-гидроксибен-зойной (салициловой) кислоты. Обработкой салициловой кислоты уксусным ангидридом получают сложный эфир салициловой кислоты — ацетилсалициловую кислоту, или аспирин:
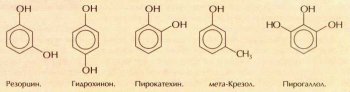
Аспирин впервые был получен в 1899 г. и сразу же после этого испытан в качестве лекарственного препарата. С тех пор эффективное и дешёвое противовоспалительное и жаропонижающее средство прочно вошло в нашу жизнь. В чистом виде это вещество плохо растворяется в воде, но некоторые фармацевтические фирмы наладили выпуск растворимого аспирина — натриевой соли ацетилсалициловой кислоты. К классу фенолов также относятся резорцин (используется в медицине), гидрохинон (применяется как восстановитель при проявлении фотоплёнок), пирокатехин (в производстве красителей, в фотографии), крезолы (в органическом синтезе), пирогаллол (основа многих дубильных веществ, используется и в химическом анализе для поглощения молекулярного кислорода).
Фрагмент деревянной постройки и маковка церкви в Кижах.

Похожие статьи