Анилин (фениламин, C6H5NH2) — бесцветная ядовитая жидкость с характерным запахом, малорастворимая в воде (tкип = 184 °С). Так назвал это вещество Ю. Ф. Фрицше, выделивший его в 1840 г. из продуктов взаимодействия краски индиго со щёлочью (от араб. «ан-нил» — «синяя краска», «индиго»). Анилин — простейший представитель ароматических аминов. В соединениях этого класса свободная электронная пара атома азота аминогруппы «затянута» в бензольное ядро. Поэтому по свойствам анилин заметно отличается и от алифатических аминов, и от бензола. Так, по сравнению с аммиаком и алкиламинами (например, метиламином CH3NH2), анилин представляет собой гораздо более слабое основание. Его водные растворы не изменяют окраски лакмуса и фенолфталеина. Однако в присутствии сильных кислот анилин, как и другие амины, образует соли (например, хлорид фениламмония [C6H5NH3]+Cl-).
Повышение электронной плотности в 2,4,6-положениях бензольного ядра приводит к тому, что анилин гораздо легче, чем бензол, вступает в реакции замещения, типичные для ароматических соединений: галогенирование, нитрование, сульфирование. Так, при взаимодействии водного раствора анилина с бромной водой выпадает белый осадок 2,4,6-триброманилина.
При хранении на воздухе анилин окисляется и превращается в тёмную вязкую жидкость. Качественной реакцией на анилин служит образование фиолетового окрашивания при окислении хлорной известью — она содержит гипохлорит кальция.
В промышленных масштабах анилин производят восстановлением нитробензола водородом. Реакция протекает в газовой фазе в присутствии катализаторов, содержащих переходные металлы — медь и никель:
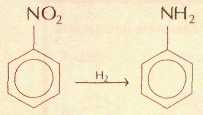
Другим методом получения анилина является аммонолиз фенола:
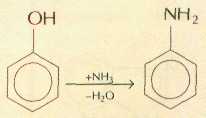
В основном анилин расходуется на производство красителей.
Похожие статьи