Простейшим представителем углеводородов с тройной связью ОС является ацетилен С2Н2. Подобно метану и этилену, ацетилен — родоначальник гомологического ряда алкинов (ацетиленовых углеводородов). Впервые этот газ был выделен в 1836 г. Эдмундом Дэви, двоюродным братом Гемфри Дэви, при разложении водой карбида калия: К2С2+2Н2О=С2Н2+2КОН, полученного при сплавлении металлического калия с углём. Эдмунд Дэви описал свойства одного из продуктов этой реакции, названного им «новым газообразным двууглеродистым водородом»: его растворимость в воде, плотность, горение на воздухе ярким коптящим пламенем, способность взаимодействовать с хлором. В 1855 г. М. Бертло получил ацетилен в разряде электрической дуги между угольными электродами в атмосфере водорода: 2С+Н2®СHºСН.
Ацетиленовая сварка.
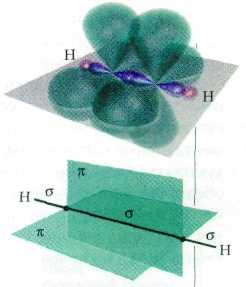
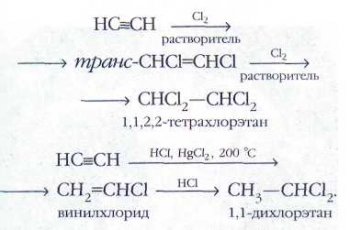
Казалось бы, раз ненасыщенность молекулы ацетилена и его гомологов больше, чем у алкенов, то и активность алкинов в реакциях присоединения должна быть выше. Однако этот вывод противоречит экспериментальным фактам: реакции с участием ацетилена и его гомологов протекают медленнее и часто лишь в присутствии катализатора. Всё дело в том, что тройная связь в ацетилене и его гомологах состоит из одной s-связи и двух p-связей. Мощная p-система дополнительно стабилизирует молекулу, поэтому реакционная способность кратной связи ацетиленовых углеводородов ниже, чем этиленовых. Реакции присоединения к алкинам протекают ступенчато:
В присутствии солей ртути ацетилен взаимодействует с водой с образованием неустойчивого винилового спирта, который изомеризуется в ацетальдегид (реакция Кучерова):
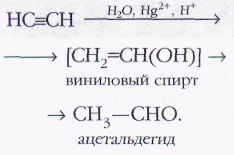
Гомологи ацетилена в этих условиях образуют кетоны:
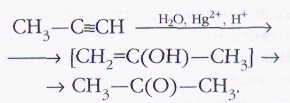
При пропускании ацетилена через раствор, содержащий хлорид аммония и взвесь хлорида меди(I), молекулы С2Н2 сдваиваются и образуется винилацетилен (бутен-З-ин-1): 2НСºСН®СН2=СН—CºСН, а в присутствии графита продуктом реакции будет бензол:

Эту реакцию открыл французский химик Марселен Бертло.
В 1839 г. в медных газопроводных трубах Нью-Йорка Джордж Торрей нашёл красное порошкообразное вещество, взрывавшееся при ударе. Сначала он решил, что ему удалось пресечь действия диверсантов, но всё оказалось гораздо сложнее: американец обнаружил ацетиленид меди(I) Cu2С2 — продукт взаимодействия ацетилена, входившего в состав газа, с соединениями меди, образовавшимися при окислении медной трубы.
Только спустя много лет учёные сумели объяснить, почему в ацетиленовых углеводородах атомы водорода при тройной связи обладают гораздо большей подвижностью, чем в алканах и алкенах. Дело в том, что атомы углерода, образующие тройную связь, имеют большую электроотрицательность и сильнее смещают к себе общую электронную пару связи С—Н. Поэтому ацетилен — не что иное, как слабая С—Н-кислота. Он взаимодействует не только со щелочными металлами: НСºСН+Na®NaCºCH+0,5H2, но и с солями меди, серебра, ртути, образуя ацетилениды. Многие из них неустойчивы — в сухом виде легко взрываются.
Ещё в 1895 г. А. Л. Ле Шателье обнаружил, что ацетилен, сгорая в кислороде даёт очень горячее пламя (до 3000 °С), поэтому его широко используют для сварки и резки тугоплавких металлов.
На основе ацетилена разработаны методы синтеза уксусного альдегида и уксусной кислоты, синтетических каучуков (изопренового и хлоропренового).
Помимо алканов, алкенов и алкинов у «чёрного золота» много других «детей» — углеводородов, содержащихся в нефти или получаемых при её переработке. К их числу относятся углеводороды циклического строения (циклоалканы, циклоалкены, ароматические углеводороды), а также непредельные углеводороды с более чем одной кратной связью.

Похожие статьи