Остеокальцин: 1) содержит 3 остатка γ-КГК → связывает Са 2+ ; 2) прочно связан с апатитом; 3) участвует в росте кристаллов.
Костный сиалопротеин: 1) содержит трипептид АРГ-ГЛИ-АСП (R-G-D) → способен связываться с другими клетками, макромолекулами и рецепторами клеточных мембран; 2) через специальный рецептор (10 остатков ГЛУ) связывается с Са 2+; 3) относится к фосфопротеинам, тесно связан с клетками и апатитом; 4) присоединяет остеобласты к кости в период ее синтеза.
Остеопонтин: 1) содержит трипептид R-G-D; 2) связывается с Са 2+; 3) прочно связан с апатитом.
Остеонектин: 1) имеет Са-связывающий домен, хотя в нем и нет γ-КГК; 2) связывается с коллагеном и апатитом.
Тромбоспондин: 1) содержит трипептид R-G-D; 2) связывается с поверхностями клеток и другими белками костной ткани.
Костный кислый гликопротеин: участвует в минерализации костной ткани.
В основе этого процесса — образование кристаллов апатита с участием фосфата кальция. В организме внеклеточная жидкость перенасыщена фосфатом кальция и он начинает осаждаться. Выделяют 2 стадии осаждения фосфата кальция:
▪нуклеация — образование плотного осадка (ядра);
▪рост кристаллов из ядра — эпитаксис.
Нуклеация бывает гомогенная (кристаллы образуются без участия другой фазы) и гетерогенная (образование кристаллов инициирует другая фаза, играющая роль матрицы- затравки). Матрица может и направлять рост кристаллов. Роль матрицы выполняют протеогликаны, гликозаминогликаны, Са-связывающие белки: фосфопротеины и белки, содержащие γ-карбоксиглутаминовую кислоту (γ-КГК), для синтеза которой нужен витамин К.
Теории минерализации костной ткани и твердых тканей зуба:
1)физико-химическая, в основе которой лежат названные выше 2 стадии;
2)ферментная: щелочная фосфатаза костной ткани гидролизует фосфорорганические эфиры, в результате этого освобождается фосфат-ион, что при наличии кальция и матрицы вызывает рост кристаллов ГА;
3)смешанная: сначала синтезируется внеклеточный матрикс, а затем наступает этап минерализации из-за перенасыщенного состояния раствора фосфата кальция и наличия матрицы.
▪нуклеация — образование плотного осадка (ядра);
▪рост кристаллов из ядра — эпитаксис.
Нуклеация бывает гомогенная (кристаллы образуются без участия другой фазы) и гетерогенная (образование кристаллов инициирует другая фаза, играющая роль матрицы- затравки). Матрица может и направлять рост кристаллов. Роль матрицы выполняют протеогликаны, гликозаминогликаны, Са-связывающие белки: фосфопротеины и белки, содержащие γ-карбоксиглутаминовую кислоту (γ-КГК), для синтеза которой нужен витамин К.
Теории минерализации костной ткани и твердых тканей зуба:
1)физико-химическая, в основе которой лежат названные выше 2 стадии;
2)ферментная: щелочная фосфатаза костной ткани гидролизует фосфорорганические эфиры, в результате этого освобождается фосфат-ион, что при наличии кальция и матрицы вызывает рост кристаллов ГА;
3)смешанная: сначала синтезируется внеклеточный матрикс, а затем наступает этап минерализации из-за перенасыщенного состояния раствора фосфата кальция и наличия матрицы.
1. Защитная.
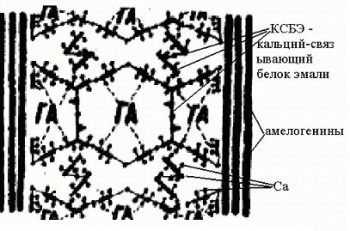
2. Минерализующая: поставщик минеральных веществ и микроэлементов в эмаль, поддерживает ее оптимальный химический состав и препятствует выходу минеральных веществ из эмали. В зрелых зубах поддерживается подвижное равновесие двух процессов: растворение эмали и ее минерализация. Константа растворимости апатитов эмали в физиологических условиях сдвинута в сторону образования кристаллов. Растворимость их зависит от концентрации ионов кальция и фосфора, рН среды, ионной силы слюны.
3. Очищающая.
4. Пищеварительная.
5. Регуляторная.
6. Выделительная.
2. Минерализующая: поставщик минеральных веществ и микроэлементов в эмаль, поддерживает ее оптимальный химический состав и препятствует выходу минеральных веществ из эмали. В зрелых зубах поддерживается подвижное равновесие двух процессов: растворение эмали и ее минерализация. Константа растворимости апатитов эмали в физиологических условиях сдвинута в сторону образования кристаллов. Растворимость их зависит от концентрации ионов кальция и фосфора, рН среды, ионной силы слюны.
3. Очищающая.
4. Пищеварительная.
5. Регуляторная.
6. Выделительная.
Муцины — защитные белки: защищают поверхность зуба от бактериального загрязнения и от растворения фосфатов кальция, придают вязкость слюне, связывая много воды.
Цистатины: ингибируют бактериальные протеазы и протеазы периодонтальных тканей.
Гистатины: богаты ГИС и являются мощными ингибиторами роста Candida albicans и Str. mutans.
Белки, богатые ПРО: содержат много Н3РО4, из-за «–» заряда тормозят рост кристаллов в слюне, связывая Са2+.
Лактоферрин: способен связывать ионы железа, лишая бактерии этого важного элемента и ограничивая их рост, хотя некоторые бактерии способны усваивать и такое, связанное с лактоферрином, железо.
Цистатины: ингибируют бактериальные протеазы и протеазы периодонтальных тканей.
Гистатины: богаты ГИС и являются мощными ингибиторами роста Candida albicans и Str. mutans.
Белки, богатые ПРО: содержат много Н3РО4, из-за «–» заряда тормозят рост кристаллов в слюне, связывая Са2+.
Лактоферрин: способен связывать ионы железа, лишая бактерии этого важного элемента и ограничивая их рост, хотя некоторые бактерии способны усваивать и такое, связанное с лактоферрином, железо.
Кутикула — после прорезывания зубов теряется.
Пелликула — тонкий слой органического материала, содержащего небольшое количество бактерий. Играет защитную функцию: многократно снижает растворимость эмали и предохраняет эмаль от повреждающего действия органических кислот. Полностью восстанавливается через 20 мин после чистки зубов, не исчезает в процессе жевания.
Зубной налет (зубная бляшка). Зубная бляшка — невидимый зубной налет. Покрыт мукоидной пленкой, поэтому устойчив к смыванию слюной и полосканию рта. Легко снимается зубной щеткой, не стирается при пережевывании пищи (исключение — твердая пища). Начинает накапливаться через 2 часа после чистки зубов. Это слой органической матрицы и бактериальных клеток на поверхности пелликулы. В зубном налете 80 % воды, 20 % — сухой остаток, из которого 40 % — минеральные вещества, а 60 % — органические. Минеральные вещества — гидрокси- и фторапатиты, СаF2. Из органических веществ главное значение имеют полисахариды: глюканы, леваны и гетерополисахариды. Зубной налет — обязательное условие развития кариеса. Быстрому образованию зубного налета способствует наличие в пище сахарозы. Компенсировать снижение рН зубного налета после приема пищи можно, стимулируя слюноотделение путем жевания сыра, орехов, жевательной резинки без сахара и с карбамидом: при этом увеличивается нейтрализующая сила слюны за счет гидрокарбонатного буфера и азотистых соединений (мочевина) и зубной налет превращается в щелочные продукты.
Пелликула — тонкий слой органического материала, содержащего небольшое количество бактерий. Играет защитную функцию: многократно снижает растворимость эмали и предохраняет эмаль от повреждающего действия органических кислот. Полностью восстанавливается через 20 мин после чистки зубов, не исчезает в процессе жевания.
Зубной налет (зубная бляшка). Зубная бляшка — невидимый зубной налет. Покрыт мукоидной пленкой, поэтому устойчив к смыванию слюной и полосканию рта. Легко снимается зубной щеткой, не стирается при пережевывании пищи (исключение — твердая пища). Начинает накапливаться через 2 часа после чистки зубов. Это слой органической матрицы и бактериальных клеток на поверхности пелликулы. В зубном налете 80 % воды, 20 % — сухой остаток, из которого 40 % — минеральные вещества, а 60 % — органические. Минеральные вещества — гидрокси- и фторапатиты, СаF2. Из органических веществ главное значение имеют полисахариды: глюканы, леваны и гетерополисахариды. Зубной налет — обязательное условие развития кариеса. Быстрому образованию зубного налета способствует наличие в пище сахарозы. Компенсировать снижение рН зубного налета после приема пищи можно, стимулируя слюноотделение путем жевания сыра, орехов, жевательной резинки без сахара и с карбамидом: при этом увеличивается нейтрализующая сила слюны за счет гидрокарбонатного буфера и азотистых соединений (мочевина) и зубной налет превращается в щелочные продукты.
По происхождению делятся на: 1) железистые; 2) лейкоцитарные; 3) микробные.
Лизоцим: бактерицидное действие основано на том, что он гидролизует гликозидную связь в гетерополисахаридах микробной оболочки и вызывает агрегацию бактерий, уменьшая их адгезию к поверхности зубов.
Пероксидазы: обязательное условие действия — наличие Н2О2 и анионов CNS‾ , Cl‾, из которых образуются ОCNS‾ и НОCl‾, действующие на аминокислоты микроорганизмов. Такие аминокислоты превращаются в токсичные альдегиды и оказывают повреждающее действие на микробы.
Нуклеазы — кислые и щелочные ДНКаза и РНКаза. Замедляют рост и размножение многих микроорганизмов в полости рта.
Десневая жидкость — это жидкое содержимое десневой бороздки. Представляет собой физиологическую среду сложного состава, содержащую лейкоциты, эпителий, микроорганизмы, электролиты, белки, ферменты. За сутки в ротовую полость поступает 0,5–2,5 мл десневой жидкости. В условиях здорового периодонта десневая жидкость — транссудат сыворотки крови, при поражении периодонта — экссудат, который образуется из-за повышения проницаемости сосудов и содержит продукты метаболизма бактерий и зубного налета.
Зубной ликвор — это жидкость, заполняющая свободные пространства всех зубных тканей. Включает в себя дентиновую и эмалевую (свободная вода эмали) жидкости. Именно через зубной ликвор и поступают все необходимые вещества для трофики зубных тканей. Белковый состав подобен белкам плазмы крови. В состав зубного ликвора входят и другие органические и неорганические молекулы. Дентиновая и эмалевая жидкости тесно связаны между собой: из дентиновой жидкости в эмалевую фильтруются различные вещества.
Лизоцим: бактерицидное действие основано на том, что он гидролизует гликозидную связь в гетерополисахаридах микробной оболочки и вызывает агрегацию бактерий, уменьшая их адгезию к поверхности зубов.
Пероксидазы: обязательное условие действия — наличие Н2О2 и анионов CNS‾ , Cl‾, из которых образуются ОCNS‾ и НОCl‾, действующие на аминокислоты микроорганизмов. Такие аминокислоты превращаются в токсичные альдегиды и оказывают повреждающее действие на микробы.
Нуклеазы — кислые и щелочные ДНКаза и РНКаза. Замедляют рост и размножение многих микроорганизмов в полости рта.
Десневая жидкость — это жидкое содержимое десневой бороздки. Представляет собой физиологическую среду сложного состава, содержащую лейкоциты, эпителий, микроорганизмы, электролиты, белки, ферменты. За сутки в ротовую полость поступает 0,5–2,5 мл десневой жидкости. В условиях здорового периодонта десневая жидкость — транссудат сыворотки крови, при поражении периодонта — экссудат, который образуется из-за повышения проницаемости сосудов и содержит продукты метаболизма бактерий и зубного налета.
Зубной ликвор — это жидкость, заполняющая свободные пространства всех зубных тканей. Включает в себя дентиновую и эмалевую (свободная вода эмали) жидкости. Именно через зубной ликвор и поступают все необходимые вещества для трофики зубных тканей. Белковый состав подобен белкам плазмы крови. В состав зубного ликвора входят и другие органические и неорганические молекулы. Дентиновая и эмалевая жидкости тесно связаны между собой: из дентиновой жидкости в эмалевую фильтруются различные вещества.
1. 99 % F в виде фторапатита входит в состав костей и зубов, придает им прочность и кислотоустойчивость.
2. Стимулирует реминерализацию костей и зубов (поступление в них кальция и фосфора).
3. Стимулирует синтез костной ткани, иммунитет (в том числе полости рта), гемопоэз.
4. Блокирует енолазу микроорганизмов (прекращается синтез лактата, который снижает рН ротовой жидкости) и синтез микроорганизмами внеклеточных полисахаридов.
5. Изменяет электрический потенциал поверхности эмали и препятствует адгезии бактерий к эмали.
Концентрация F выражается в мг/л и ppm (parts per million): 1 мг/л = 1 ppm; 1 % = 10000 ppm.
Рекомендации Всемирной организации здравоохранения (ВОЗ), 1994 г.:
за оптимум принято количество F, приближающееся к 4 мг/сут (1,5–4 мг/сут);
1,2 мг F — из воды (30 %); 2,0 мг — из пищи (50 %); 0,8 мг — из воздуха (20 %);
в жарких странах F в воде должно быть 0,5–0,8 мг/л, с умеренным климатом — 0,8– 1,0 мг/л, в северных — 1,0–1,2 мг/л.
Больше всего F в морепродуктах, зеленом и черном чае, красном вине. Много F в районах комбинатов по выпуску фосфорных удобрений, сжигания каменного угля.
2. Стимулирует реминерализацию костей и зубов (поступление в них кальция и фосфора).
3. Стимулирует синтез костной ткани, иммунитет (в том числе полости рта), гемопоэз.
4. Блокирует енолазу микроорганизмов (прекращается синтез лактата, который снижает рН ротовой жидкости) и синтез микроорганизмами внеклеточных полисахаридов.
5. Изменяет электрический потенциал поверхности эмали и препятствует адгезии бактерий к эмали.
Концентрация F выражается в мг/л и ppm (parts per million): 1 мг/л = 1 ppm; 1 % = 10000 ppm.
Рекомендации Всемирной организации здравоохранения (ВОЗ), 1994 г.:
за оптимум принято количество F, приближающееся к 4 мг/сут (1,5–4 мг/сут);
1,2 мг F — из воды (30 %); 2,0 мг — из пищи (50 %); 0,8 мг — из воздуха (20 %);
в жарких странах F в воде должно быть 0,5–0,8 мг/л, с умеренным климатом — 0,8– 1,0 мг/л, в северных — 1,0–1,2 мг/л.
Больше всего F в морепродуктах, зеленом и черном чае, красном вине. Много F в районах комбинатов по выпуску фосфорных удобрений, сжигания каменного угля.
1. Гомеостатическая. Поддерживает постоянный состав крови (гомеостаз). Питательные вещества в желудочно-кишечном тракте всасываются периодически. Их концентрации в портальном кровотоке в разные периоды времени существенно различаются, но благодаря гомеостатической функции печени концентрации важнейших метаболитов в большом круге кровообращения практически постоянны.
2. Роль печени в обмене белков. Освобождающиеся в процессе пищеварения аминокислоты попадают с током крови в печень и используются для:
синтеза белков плазмы крови (альбуминов, глобулинов, факторов свёртывания крови); образования α-кетокислот путём трансаминирования или окислительного дезаминирования аминокислот;
глюконеогенеза;
синтеза кетоновых тел;
получения энергии, подвергаясь превращениям в цикле трикарбоновых кислот;
синтеза мочевины;
синтеза креатина, холина.
2. Роль печени в обмене белков. Освобождающиеся в процессе пищеварения аминокислоты попадают с током крови в печень и используются для:
синтеза белков плазмы крови (альбуминов, глобулинов, факторов свёртывания крови); образования α-кетокислот путём трансаминирования или окислительного дезаминирования аминокислот;
глюконеогенеза;
синтеза кетоновых тел;
получения энергии, подвергаясь превращениям в цикле трикарбоновых кислот;
синтеза мочевины;
синтеза креатина, холина.
Мышцы составляют у взрослого человека 40 % от массы тела.
Функция мышц — напряжение и укорочение с последующим расслаблением.
Значение мышц — обеспечение подвижности организма и сопротивление механической силе, в том числе и статические нагрузки.
Механизм работы мышц — превращение химической энергии в механическую.
К мышечной ткани относятся:
▪скелетная мускулатура;
▪сердечная мышца;
▪гладкая мускулатура.
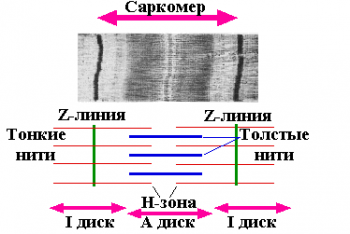
Скелетная и сердечная мышцы под микроскопом имеют поперечно-полосатое строение, а гладкая — нет. Мышечные клетки состоят из миофибрилл, а функциональной единицей миофибрилл является саркомер.
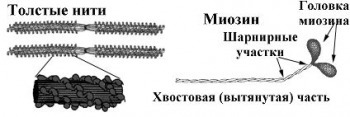
1. Миозин — основа толстых нитей. Молекулярная масса ≈ 500.000 Да. Молекула миозина имеет вытянутую часть, состоящую из двух спиралей, накрученных одна на другую. Каждая спираль имеет на одном конце глобулярную головку и называется тяжёлой цепью. Возле головок спиралей располагается по 2 лёгких цепи.
При обработке ферментами молекула миозина распадается на 2 больших фрагмента: тяжёлый меромиозин (обе головки и часть двойной спирали) и лёгкий меромиозин (остальная часть двойной спирали).
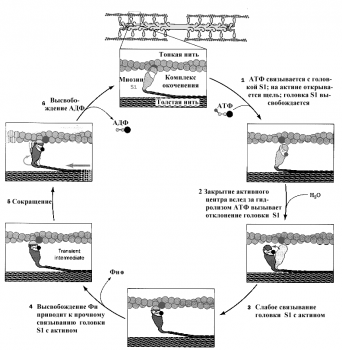
В ответ на нервный импульс происходит выброс ионов кальция из саркоплазматического ретикулума (СПР). Эти ионы связываются с лёгкими цепями миозина, при этом в головке расщепляется АТФ и головка готова присоединиться к актину. Ионы кальция затем связываются с тропонином С и меняют его конформацию. Эти изменения в силу эффекта кооперации передаются на субъединицу I и блокируют её. Далее изменения достигают субъединицы Т, которая и сдвигает в сторону молекулу тропомиозина, освобождая сразу 7 молекул актина. Головка миозина соединяется с актином, и образуется «поперечный мостик». Как только это произошло, АДФ и Фн уходят, головка наклоняется в сторону М-линии и тянет за собой тонкую нить. Затем к головке миозина присоединяется новая молекула АТФ, головка отделяется от нити актина, а гидролиз АТФ возвращает головку в вертикальное положение. Далее всё повторяется. Информацией о конце сокращения служит снижение концентрации ионов кальция в СПР. Тогда кальциевый насос и белок кальсеквестрин убирают избыток ионов кальция из цитоплазмы в СПР. Мышца переходит в состояние покоя.
1.Основной регулятор энергетики мышечной клетки — это отношение [АТФ]/ [АДФ]∙[Фн]. В покое концентрация АТФ высокая, а АДФ — низкая, в результате чего тормозится активность ключевых ферментов гликолиза, цикла Кребса и работа дыхательной цепи. С началом работы мышц концентрация АТФ падает, а АДФ возрастает, что приводит к активации вышеназванных процессов.
2.Накапливающийся при работе мышц лактат поступает из крови в печень, где путём глюконеогенеза превращается в глюкозу, которая поступает сначала в кровь, а затем в мышцы, где восстанавливает запас гликогена.
3.Аденилаткиназная (миокиназная) реакция:
2 АДФ ↔ АТФ + АМФ.
АТФ используется для мышечного сокращения, а АМФ стимулирует гликолиз.
4.Креатинкиназная реакция:
Креатин + АТФ↔КФ + АДФ.
Покоящиеся мышцы содержат в 10–20 раз больше КФ, чем АТФ, но КФ, в отличие от АТФ, не может использоваться мышцами для сокращения. Роль КФ заключается в том, что он является не только транспортной формой энергии в мышцах, но и отдаёт свою богатую энергией связь АДФ для образования АТФ, который и расходуется при сокращении. Это система быстрого реагирования: она включается первой при нехватке АТФ в мышцах. Запаса КФ хватает только на 10 с, но за это время запускаются 1–3-й механизмы. Особенно эта система важна для миокарда, так как он очень чувствителен к недостатку кислорода и имеет исключительно аэробный характер обмена в отличие от скелетной мускулатуры.
2.Накапливающийся при работе мышц лактат поступает из крови в печень, где путём глюконеогенеза превращается в глюкозу, которая поступает сначала в кровь, а затем в мышцы, где восстанавливает запас гликогена.
3.Аденилаткиназная (миокиназная) реакция:
2 АДФ ↔ АТФ + АМФ.
АТФ используется для мышечного сокращения, а АМФ стимулирует гликолиз.
4.Креатинкиназная реакция:
Креатин + АТФ↔КФ + АДФ.
Покоящиеся мышцы содержат в 10–20 раз больше КФ, чем АТФ, но КФ, в отличие от АТФ, не может использоваться мышцами для сокращения. Роль КФ заключается в том, что он является не только транспортной формой энергии в мышцах, но и отдаёт свою богатую энергией связь АДФ для образования АТФ, который и расходуется при сокращении. Это система быстрого реагирования: она включается первой при нехватке АТФ в мышцах. Запаса КФ хватает только на 10 с, но за это время запускаются 1–3-й механизмы. Особенно эта система важна для миокарда, так как он очень чувствителен к недостатку кислорода и имеет исключительно аэробный характер обмена в отличие от скелетной мускулатуры.