История энзимологии: В 1814 году Кирхгоф открыл, что солод ячменя вызывает броже ние крахмала. Дальнейшее развитие ферментологии связано с именами Либиха, Пастера, Манасеиной, Лебедева. В 1913 году Ментен и Михаэлис выдвинули теорию механизма дей ствия ферментов. В 1926 году (год рождения ферментологии как науки) Самнер выделил кристаллическую уреазу и доказал ее белковую природу. В 1969 году Меррифильд (Нью Йорк) синтезировал искусственно рибонуклеазу.
Общие понятия энзимологии. Ферменты (энзимы) – это биокатализаторы преимущест венно белковой природы (иРНК тоже имеют ферментативную активность), которые при нимают участие в химических реакциях в организме.
Слово «фермент» происходит от слова «fermentatio» брожение, а энзим – от «enzyme», что означает закваска в дрожжах. Наука, изучающая ферменты, называется энзимологией или ферментологией.
Принятые обозначения в энзимологии: Е – фермент, энзим (“еnzуме”).
S – субстрат – вещество, на которое действует фермент.
Р – продукт реакции – вещество, образовавшееся в результате ферментативной реакции
Значениеферментов: ферменты принимают участие в большинстве процессов проис ходящих в организме – 1) реакциях синтеза и распада веществ, 2) процессах переваривания и всасывания, 3) освобождения энергии, 4) обеспечивают координацию биохимических реак ций. Нарушение синтеза или активности ферментов приводит к возникновению болезней.
Слово «фермент» происходит от слова «fermentatio» брожение, а энзим – от «enzyme», что означает закваска в дрожжах. Наука, изучающая ферменты, называется энзимологией или ферментологией.
Принятые обозначения в энзимологии: Е – фермент, энзим (“еnzуме”).
S – субстрат – вещество, на которое действует фермент.
Р – продукт реакции – вещество, образовавшееся в результате ферментативной реакции
Значениеферментов: ферменты принимают участие в большинстве процессов проис ходящих в организме – 1) реакциях синтеза и распада веществ, 2) процессах переваривания и всасывания, 3) освобождения энергии, 4) обеспечивают координацию биохимических реак ций. Нарушение синтеза или активности ферментов приводит к возникновению болезней.
Образование Н2O2 и СО2.
Напомним, что тканевое дыхание это процесс поглощения кислорода (О2) тканями при окислении органического субстрата с выделением углекислого газа и воды. Выше мы уже показали, как из атомов водорода в дыхательной цепи образуются молекулы воды. Однако процесс дегидрирования субстрата НАД и ФАДзависимыми дегидрогеназами одновременно ведет и к отщеплению концевой карбоксильной группы, которая выделяется в виде СО2. Главными источниками СО2 является реакции декарбоксилирования пировиноградной и альфакетоглутаровой кислот (см. выше). Еще один источник – это процесс декарбоксилиро вание аминокислот, который катализируется пиридоксальзависимыми ферментами.
Поглощенный клеткой кислород в основном (до 8090%) используется для производства энергии в митохондриях. Однако, кислород используется и на другие цели – для синтеза сте роидов, простагландинов, лейкотриенов, тирозина, катехоламинов, для метаболизма чуже родных веществ и т.д.. При этом часть поглощенного тканями кислорода неферментативным путем или при участии монооксигеназ способна превращаться в активные формы (суперок сидный, гидроксильный. пероксильный радикалы, синглетный кислород, пероксид водорода, органическое пероксиды)
Напомним, что тканевое дыхание это процесс поглощения кислорода (О2) тканями при окислении органического субстрата с выделением углекислого газа и воды. Выше мы уже показали, как из атомов водорода в дыхательной цепи образуются молекулы воды. Однако процесс дегидрирования субстрата НАД и ФАДзависимыми дегидрогеназами одновременно ведет и к отщеплению концевой карбоксильной группы, которая выделяется в виде СО2. Главными источниками СО2 является реакции декарбоксилирования пировиноградной и альфакетоглутаровой кислот (см. выше). Еще один источник – это процесс декарбоксилиро вание аминокислот, который катализируется пиридоксальзависимыми ферментами.
Поглощенный клеткой кислород в основном (до 8090%) используется для производства энергии в митохондриях. Однако, кислород используется и на другие цели – для синтеза сте роидов, простагландинов, лейкотриенов, тирозина, катехоламинов, для метаболизма чуже родных веществ и т.д.. При этом часть поглощенного тканями кислорода неферментативным путем или при участии монооксигеназ способна превращаться в активные формы (суперок сидный, гидроксильный. пероксильный радикалы, синглетный кислород, пероксид водорода, органическое пероксиды)
Патология тканевого дыхания. Различают ингибиторы электронного транспорта, ингибиторы и разобщители окислительного фосфорилирования в митохондриях.
а) ингибиторы электронного транспорта – это вещества, которые взаимодействуют с компонентами дыхательной цепи и нарушают транспорт электронов по ней. Они являются клеточными токсинами, вызывают тканевую гипоксию. К ним относятся: 1) Ротенон (инсек тицид), снотворные препараты амобарбитал (амитал) и секобарбитал – тормозит транспорт электронов через НАДНКоQредуктазу; 2) Пиерицидин А (антибиотик), блокирует НАД Н КоQредуктазу; 3) Антимицин А (антибиотик), блокирует дыхательную цепь на уровне III комплекса (цитохром b–цитохром с); 4) Цианиды (ионы СN) – образуют комплексы с Fe3+ цитохромоксидазы, тормозят восстановление до Fe2+ в ЦХО; 5) Монооксид углерода (СО) – блокирует ЦХО, связываясь с гемом тормозит его взаимодействие с кислородом.
Тканевое дыхание угнетается также в том случае, если в организм с пищей поступает недостаточное количество витаминов РР и В2 (эти витамины являются предшественниками НАД и ФМН), а также микроэлементов железа и меди (Fe и Cu входят в состав цитохромов).
а) ингибиторы электронного транспорта – это вещества, которые взаимодействуют с компонентами дыхательной цепи и нарушают транспорт электронов по ней. Они являются клеточными токсинами, вызывают тканевую гипоксию. К ним относятся: 1) Ротенон (инсек тицид), снотворные препараты амобарбитал (амитал) и секобарбитал – тормозит транспорт электронов через НАДНКоQредуктазу; 2) Пиерицидин А (антибиотик), блокирует НАД Н КоQредуктазу; 3) Антимицин А (антибиотик), блокирует дыхательную цепь на уровне III комплекса (цитохром b–цитохром с); 4) Цианиды (ионы СN) – образуют комплексы с Fe3+ цитохромоксидазы, тормозят восстановление до Fe2+ в ЦХО; 5) Монооксид углерода (СО) – блокирует ЦХО, связываясь с гемом тормозит его взаимодействие с кислородом.
Тканевое дыхание угнетается также в том случае, если в организм с пищей поступает недостаточное количество витаминов РР и В2 (эти витамины являются предшественниками НАД и ФМН), а также микроэлементов железа и меди (Fe и Cu входят в состав цитохромов).
Окислительное фосфорилирование – это процесс образования АТФ из АДФ и неоргани ческого фосфата (Фн) в процессе тканевого дыхания. Согласно хемиосмотической теории Митчела синтез АТФ осуществляется за счет електрохимического потенциала, который созда ется градиентом концентраций ионов водорода. Комплексы I, III и IV расположены асимметрич но во внутренней мембране митохондрий и обра зуют 3 петли, которые обеспечивают перекачи вания протонов из матрикса митохондрий в межмембранное пространство. То есть комплек сы I, III и IV по сути служат протонными насоса ми. С каждой парой электронов, которые пере даются от субстрата к кислороду, эти три петли транспортируют в межмебранное простран ство 810 протонов (Н+). Источником протонов является диссоциация эндогенной воды: Н2O→Н++ОН, а энергия необходимая для транспорта ионов Н+ черпается за счет движения электронов. В матриксе накапливаются гидроксиданионы ОН, а в межмембранном про странстве ионы Н+ т.е. формируется трансмембранный электрохимический градиент кон центрации ионов Н+ – ∆µН+. Внешняя поверхность внутренней мембраны, обращенная в межмембранное пространство, заряжается положительно (+), а внутренняя отрицательно (). Внутренняя мембрана митохондрий непроницаема для ионов Н+, однако, они могут прохо дить назад в матрикс через протонный канал (фрагмент Fо) Н+АТФсинтазы. Второй фрагмент F1 фермента является каталитическим и осуществляет синтез АТФ. Каталитиче ская часть АТФсинтазы катализирует три последовательные стадии синтеза АТФ. Вначале идет связывание АДФ и неорганического фосфата (1 стадия), затем образуется фосфоангид ридная связь (2 стадия) и, наконец, освобождается конечный продукт реакции (3 стадия).
Редокспотенциал (РОП) – это величина электрического заряда, которая создается между платиновыми электродами, помещенными в раствор, содержащий окисленную и вос становленную форму вещества. Редокспотенциалы различных веществ приравнивают к во дородному потенциалу, величина которого принята за 0. Величины редокспотенциалов компонентов дыхательной цепи показы вают порядок движения электронов, на чиная с окисляемого субстрата (SН2), имеющего редокспотенциал 0,7V и заканчивая кислородом с редокс потенциалом +0,8V. Таким образом, электроны движутся по направлению от субстрата к кислороду, т.е. от соедине ний с меньшим редокспотенциалом к большему. При пересчете РОП в энер гию (уравнение ∆G= nF.∆E0) общий пе репад энергии в дыхательной цепи ра вен 220 кДж В дыхательной цепи имеются пункты где перепады РОП особенно велики. Так, на участке НАДН2 –коэнзим Q (комплекс I) изменение РОП составляет 0,27V, на участке ци тохром b – цитохром с (комплекс III) – 0,22V, и на участке цитохром а3 – О2 (комплекс IV) – 0,53V, что соответствует энергии, соответственно, 51,0, 41,4 и 99,6 кДж. Этой энергии доста точно для синтеза 3х молекул АТФ (синтез 1 молекулы АТФ требует затрат 30,5 кДж
Внешняя мембрана митохондрий – играет разграничитель ную роль, в ней содержатся ферменты удлинения насыщенных жирных кислот, кинуренин гидроксилаза, МАО (маркерный фермент) и др. Межмембранное пространство (ММП) – содержит аденилатциклазу и нуклеозиддифосфаткиназу). Внутренняя мембрана содержит ферменты тканевого дыхания. Маркерный фермент цитохромоксидаза. Матрикс (М) содер жит ферменты ЦТК, βокисления жирных кислот, декарбоксилирования альфа–кетокислот.
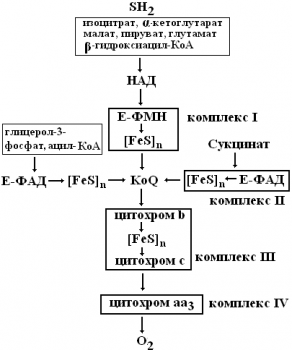
Дыхательня цепь – это система ферментов и коферментов, которые принимают уча стие в транспорте электронов и протонов от окисляемого субстрата к кислороду. Дыхатель ная цепь включает: а) ферменты: НАД или ФМН(ФАД)зависимые дегидрогеназы; цито хромы (гемопротеины, содержащие простетическую группу гем); б) коферменты: НАД, ФМН, КоQ, гем. в) електронотранспортные белки (железосерные белки).
Дыхательня цепь – это система ферментов и коферментов, которые принимают уча стие в транспорте электронов и протонов от окисляемого субстрата к кислороду. Дыхатель ная цепь включает: а) ферменты: НАД или ФМН(ФАД)зависимые дегидрогеназы; цито хромы (гемопротеины, содержащие простетическую группу гем); б) коферменты: НАД, ФМН, КоQ, гем. в) електронотранспортные белки (железосерные белки).
История развития учения о биологическом окислении
1. Теория активации кислорода (А.Н.Бах). Согласно этой теории непосредственным агентом, окисляющим субстрат является активированный кислород. Активация молекуляр ного кислорода осуществляется особыми ферментами оксигеназами и ведет к образованию реакционноспособных пероксидов, которые при участии ферментов пероксидаз и взаи модействуют с субстратом.
В дальнейшем оказалось, что действительно в клетках существует ферменты, способные активировать молекулярный кислород и использовать его для окисления ряда веществ. Су ществуют ферменты монооксигеназы, которые присоединяют к субстрату один атом кисло рода (SH +1/2 O2 → SOH ) и диоксигеназы, которые присоединяют к субстрату 2 атома ки слорода (S + O2 → SO2). Монооксигеназы и диоксигеназы катализируют реакции гидрокси лирования стероидов, ксенобиотиков, образование простагландинов и лейкотриенов, но не принимают участия в процессах биологического окисления в митохондриях.
1. Теория активации кислорода (А.Н.Бах). Согласно этой теории непосредственным агентом, окисляющим субстрат является активированный кислород. Активация молекуляр ного кислорода осуществляется особыми ферментами оксигеназами и ведет к образованию реакционноспособных пероксидов, которые при участии ферментов пероксидаз и взаи модействуют с субстратом.
В дальнейшем оказалось, что действительно в клетках существует ферменты, способные активировать молекулярный кислород и использовать его для окисления ряда веществ. Су ществуют ферменты монооксигеназы, которые присоединяют к субстрату один атом кисло рода (SH +1/2 O2 → SOH ) и диоксигеназы, которые присоединяют к субстрату 2 атома ки слорода (S + O2 → SO2). Монооксигеназы и диоксигеназы катализируют реакции гидрокси лирования стероидов, ксенобиотиков, образование простагландинов и лейкотриенов, но не принимают участия в процессах биологического окисления в митохондриях.
Биологическое окисление это процесс окисления биологических веществ с выделением энергии.
Тканевое дыхание – процесс поглощения кислорода (О2) тканями при окислении орга нического субстрата с выделением углекислого газа (СО2) и воды (Н2О). Окислительное фосфорилирование это синтез АТФ сопряженный с тканевым дыханием.
Основным топливом при биологическом окислении является водород. Известно, что ре акция окисление водорода кислородом в газовой среде сопровождается выделением большо го количества энергии, сопровождаемым взрывом и пламенем. Эволюция живых организмов привела к тому, что реакция окисления водорода до воды оказалась разделенной на отдель ные этапы, что обеспечивает постепенное высвобождение энергии в процессе биологическо го окисления. При этом часть полученной энергии рассеивается в виде тепла (около 60%) а другая часть (около 40%) аккумулируется в молекулах АТФ.
Тканевое дыхание – процесс поглощения кислорода (О2) тканями при окислении орга нического субстрата с выделением углекислого газа (СО2) и воды (Н2О). Окислительное фосфорилирование это синтез АТФ сопряженный с тканевым дыханием.
Основным топливом при биологическом окислении является водород. Известно, что ре акция окисление водорода кислородом в газовой среде сопровождается выделением большо го количества энергии, сопровождаемым взрывом и пламенем. Эволюция живых организмов привела к тому, что реакция окисления водорода до воды оказалась разделенной на отдель ные этапы, что обеспечивает постепенное высвобождение энергии в процессе биологическо го окисления. При этом часть полученной энергии рассеивается в виде тепла (около 60%) а другая часть (около 40%) аккумулируется в молекулах АТФ.
Анаплеротические реакции – это реакции клеточного метаболизма, повышающие кон центрацию субстратов ЦТК, образуя их в других метаболических путях.
Например:
1.Образование α кетоглутарата и оксалоацетата в реакциях трансаминирования аминокислот;
2.Образование α–кетоглутарата в глутаматдегидрогеназной реакции;
3.Образование ок салоацетата из пирувата в пируваткарбоксилазной реакции.
Например:
1.Образование α кетоглутарата и оксалоацетата в реакциях трансаминирования аминокислот;
2.Образование α–кетоглутарата в глутаматдегидрогеназной реакции;
3.Образование ок салоацетата из пирувата в пируваткарбоксилазной реакции.
Гидрогендонорное. Реакции дегидрирования происходящие в ЦТК служат источни ком атомов водорода (НАДН2) для дыхательной цепи. В ЦТК образуется и НАДФН2 (НАДФ зависимые изоцитрат и малатдегидрогеназы), который далее используется как восстанови тель при синтезе жирных кислот, стероидных гормонов, окислении ксенобиотиков.
Энергетический баланс ЦТК. В ЦТК образуется 2 молекулы СО2 (в изоцитратдегид рогеназной и αкетоглутаратдегидрогеназной реакциях) и 3 молекулы НАДН2 и одна молекула ФАДН2. Окисление НАДН2 в дыхательной цепи митохондрий дает по 3 молекулы АТФ на каждую молекулу НАДН2 и по 2 молекулы АТФ на каждую молекулу ФАДН2. Одна мо лекула АТФ образуется за счет субстратного фосфорилирования на этапе превращении сук цинилКоА в сукцинат. Таким образом, при полном окислении 1 молекулы ацетилКоА до СО2 и Н2О генерируется 12 молекул АТФ.
ЦТК регулируется через изменение активности аллостерических ферментов цитратсин тетазы; изоцитратдегидрогеназы; альфа–кетоглутаратдегидрогеназы. Они активируются АДФ, но ингибируются АТФ, НАДН2, сукцинил–КоА, длинноцепочечными ацил–КоА.
Значение ЦТК. 1.Интегративное – цикл Кребса объединяет пути катаболизма углеводов, белков и жиров, т.к. в нем утилизируется молекулы ацетилКоА, образующиеся при расщеплении этих веществ.
2.Энергетическое. При расщеплении 1 молекулы ацетилКоА до конечных продуктов (СО2 и Н2О) генерируется 12 молекул АТФ.
3.Амфиболическое (двойственное). В ЦТК происходит не только катаболические процессы – окисление ацетилКоА. Субстраты ЦТК используются и для реакций синтеза (анабо лические процессы). Так, из оксалоацетата синтезируется аспарагиновая кислота; из α кетоглутаровой кислоты – глутаминовая; из оксалоацетата фосфоэнолпируват.
ЦТК регулируется через изменение активности аллостерических ферментов цитратсин тетазы; изоцитратдегидрогеназы; альфа–кетоглутаратдегидрогеназы. Они активируются АДФ, но ингибируются АТФ, НАДН2, сукцинил–КоА, длинноцепочечными ацил–КоА.
Значение ЦТК. 1.Интегративное – цикл Кребса объединяет пути катаболизма углеводов, белков и жиров, т.к. в нем утилизируется молекулы ацетилКоА, образующиеся при расщеплении этих веществ.
2.Энергетическое. При расщеплении 1 молекулы ацетилКоА до конечных продуктов (СО2 и Н2О) генерируется 12 молекул АТФ.
3.Амфиболическое (двойственное). В ЦТК происходит не только катаболические процессы – окисление ацетилКоА. Субстраты ЦТК используются и для реакций синтеза (анабо лические процессы). Так, из оксалоацетата синтезируется аспарагиновая кислота; из α кетоглутаровой кислоты – глутаминовая; из оксалоацетата фосфоэнолпируват.