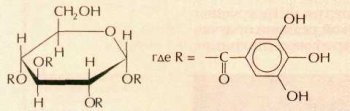Одна из основных операций при выработке кожи и меха — дубление. Так принято называть обработку шкур специальными веществами, делающими поверхность материала более прочной и упругой.
Кожа состоит из тонких волокон белка коллагена, образующих своеобразную сетчатую структуру. Эта структура и придаёт коже упругость. В результате дубления между отдельными волокнами коллагена образуются поперечные связи, и возникает более прочная пространственная структура. Дублёная кожа устойчивее к внешним воздействиям и меньше подвержена набуханию.
В качестве дубильных веществ используют органические и неорганические соединения. К органическим относятся таниды, содержащиеся в коре и листьях некоторых деревьев и кустарников, где они образуются из углеводов и фенолов. Больше всего танидов (10,5 %) в коре молодого дуба, из которой делают экстракт, применяемый при дублении
Простейший представитель класса фенолов — соединение, давшее название всему классу, С6Н5ОН. Это бесцветное кристаллическое вещество (tплав=41 °С) с характерным запахом, плохо растворимое в холодной воде. Попав на кожу, фенол вызывает ожоги, поэтому обращаться с ним нужно осторожно.
Источник фенола — каменноугольная смола, из которой он был впервые выделен в 1834 г. В наше время его получают из бензола и пропилена — кумольным способом, разработанным в 1949 г. советским химиком Рудольфом Юрьевичем Удрисом.
По химическим свойствам фенол отличается от спиртов и бензола. Это слабая кислота, и долгое время его называли карболовой кислотой. Фенол обладает бактерицидным действием — он убивает даже самые стойкие бактерии и микроскопические грибки. Поэтому его водный 5-процентный раствор широко применяли для дезинфекции помещений.
Впервые образование блестящих шелковистых кристаллов наблюдал при сухой перегонке смол алхимик Андреас Либавий. Оказалось, что это бензойная кислота C6H5COOH — вещество, в холодной воде плохо растворимое, а в горячей — хорошо. Сама кислота и её сложные эфиры входят в состав многих эфирных масел (например, гвоздичного) и бальзамов. Содержащие бензойную кислоту ягоды брусники и клюквы могут долго храниться, поскольку почти не подвержены гниению. Дело в том, что бензойная кислота убивает болезнетворные бактерии, вызывающие гниение. Благодаря этому свойству, а также нетоксичности бензойную кислоту и её соли (например, бензоат натрия) активно используют в качестве консерванта в пищевой промышленности — добавляют во фруктовые соки, соусы, джемы, безалкагольные напитки.
Учёные XIX в., опиравшиеся только на теорию химического строения А. М. Бутлерова, не смогли решить все загадки молекулы бензола и чётко определить понятие ароматичности. Тогда ароматическим считалось любое органическое вещество, в молекуле которого содержится бензольное ядро. Но уже в начале XX столетия были открыты небензоидные соединения, по свойствам, весьма похожие на бензол и его производные, но не содержащие в своих молекулах бензольного цикла. Этих веществ становилось всё больше, вот почему теория органической химии остро нуждалась в чётких критериях ароматичности того или иного соединения.
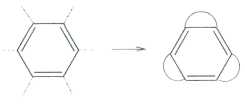
Бензол Тиле.
Что такое С6Н6? Любой химик, не задумываясь, скажет — бензол! А собственно, почему? У соединения С6Н6, как и у большинства углеводородов, должны быть изомеры, причём на бензол вовсе не похожие (всего их 217!). А сколько существует валентных изомеров бензола, т. е. таких, которые можно перевести друг в друга, «не трогая» атомы, а лишь за счёт перераспределения между ними химических связей? У всех валентных изомеров бензола каждый атом углерода должен быть соединён только с одним атомом водорода. Некоторые из этих структур предлагались ещё в XIX в. Самые известные — бензол Кекуле (1) и бензол Дьюара (2).
Английский физик и химик Джеймс Дьюар (1842—1923) в 1867 г. выступил на заседании Королевского общества в Эдинбурге с лекцией «Об окислении фенилового спирта и механическом устройстве, иллюстрирующем структуру ненасыщенных углеводородов». Он рассказал об устройстве, состоящем из стержней и шариков, с помощью которых можно конструировать модели органических молекул. Для иллюстрации потенциальных возможностей своего изобретения учёный сконструировал модель «бензола Кекуле», а также ещё несколько изомеров. Один из них — структура (2) — впоследствии получил название «дьюаровского бензола»: некоторые химики полагали, что именно таково строение этого соединения. Правда, сам Дьюар никогда не заявлял, что какая-либо из его моделей может описывать строение «настоящего» бензола.