ФИЗИЧЕСКИЙ ПРОЦЕСС И ХИМИЧЕСКАЯ РЕАКЦИЯ
Если бы миллионы разнообразных веществ, а следовательно, и тела, из них состоящие, не претерпевали никаких изменений, мир был бы скучным и застывшим, лишённым движения, развития. К счастью, мир устроен иначе. Под воздействием внешних условий (температуры, давления, освещённости и др.) вещества изменяются. Вода закипает и переходит в пар, лёд тает, распускаются и опадают листья, расцветают и увядают цветы. Течёт жизнь...
Изменения веществ и тел обычно подразделяют на два типа: физические процессы и химические превращения (реакции).
Физический процесс не затрагивает молекул (или других мельчайших структурных единиц) веществ. Их химический состав остаётся прежним, меняется лишь форма тела (при деформации), размер частичек (при измельчении вещества), агрегатное состояние. Кипение воды, вытягивание алюминиевой проволоки, появление инея, выпадение росы, образование тумана, измельчение мрамора — всё
это физические процессы. При этом молекулы воды не распадаются на атомы, атомы алюминия не объединяются в молекулы.
А вот явления, в ходе которых одни вещества превращаются в другие, называют химическими превращениями или химическими реакциями. Они тоже знакомы каждому: горение древесины, ржавление железа, прогоркание масла, скисание молока... Химическая реакция — это взаимодействие частиц (молекул, атомов) вещества или разных веществ друг с другом, которое приводит к разрыву старых и образованию новых химических связей. При этом изменяется строение молекул исходных веществ и, как правило, состав (есть и такие химические реакции, при которых состав вещества не меняется, например превращение графита в алмаз).
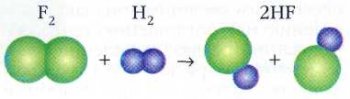
В химической реакции происходит перераспределение химических связей: старые — рвутся, новые — образуются.
Образование инея — пример физического процесса.
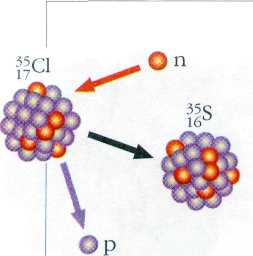
В ядерной реакции, в отличие от химической, происходит изменение зарядов ядер атомов: 3517Cl+10n®3516S+11p.
Выделение газа может сопровождать не только химическую реакцию.
Химические превращения, как правило, протекают с выделением или поглощением энергии, обычно в виде теплоты (за исключением немногочисленных термонейтральных реакций, имеющих нулевой тепловой эффект). Некоторые реакции, например горение, сопровождаются выделением света.
При химических реакциях строение атомов всегда остаётся неизменным. В этом главное отличие химических процессов от ядерных, в ходе которых ядра атомов перестраиваются, и один элемент может превратиться в другой, например алюминий — в натрий, хлор — в серу и т. д. Выделяющаяся при этом энергия может достигать колоссальных значений, как происходит при ядерном взрыве.
Химические превращения записывают с помощью уравнений. Вещества, расположенные слева от знака равенства, называют исходными веществами или реагентами, а представленные в правой части уравнения — продуктами химической реакции. Количества атомов каждого элемента в левой и правой части должны совпадать (ведь атомы не возникают и не исчезают в результате химических превращений, они лишь переходят из одного соединения в другое). Уравнивают их с помощью коэффициентов — цифр, указывающих, сколько частиц вступает в реакцию. Некоторые физические процессы, например плавление льда, также можно представить в виде уравнений, но с указанием агрегатного состояния веществ: Н2О(тв) ® Н2О(ж).


Похожие статьи