Уважаемые читатели, когда нам кто-нибудь говорит о пирамидах, то мы, прежде всего, вспоминаем Египет и Мексику. Однако древние пирамиды встречаются на всех материках и почти во всех странах мира. Четырехгранные пирамиды правильных пропорций, возведенные еще до Потопа, и по сей день стоят на Канарских островах, в Гватемале, Сальвадоре, Гондурасе, в Японии и Перу, в Монголии и Китае, на Тибете и во многих местах России. Пирамиды находят на Украине, в Индонезии, Болгарии, Иране, в Бразилии, Индии, Таиланде и многих-многих других странах. Кроме наземных пирамид в последние годы люди открыли еще и множество подводных пирамид. Некоторые подводные пирамиды изготовлены из прозрачных материалов, напоминающих стекло. Пирамидальные строения из камня наши предки сооружали в местах выхода на поверхность Земли мощных потоков теллурической энергии. Пирамиды строились в горах, в низинах, на дне морей, над разломами земной коры. Конструкции четырехгранных пирамид, обнаруженных учеными, отличаются соотношением высоты к длине основания, ступенчатостью и «срезанными» вершинами. От конструкции пирамиды зависит мощность и качество ее воздействия на людей, на землю, на искривление времени и пространства вокруг строения, зависят ее защитные функции и еще многое другое. А вы знаете, дорогие мои, что пирамиды стоят даже на других планетах. Огромные пирамиды были обнаружены американскими спутниками на Марсе, на Венере, на Юпитере. Даже на Луне недавно были сфотографированы несколько гигантских пирамид индийским спутником, например, пирамида в центре кратера Альфонс. Кроме того, каждый год водолазы обнаруживают на дне земных морей и озер громадные подводные пирамиды. Для какой же цели древние люди и боги (представители инопланетных цивилизаций) воздвигали на всех континентах и крупных островах, во всех уголках Земли свои правильные четырехгранные пирамиды? И почему атлантами выбрана форма четырехгранных пирамид, построенных по Золотому сечению?
Мышьякорганические соединения вполне могут считаться «патриархами» среди элементоорганических соединений. Их история началась ещё в 1760 г., когда фармацевт французской армии Луи Клод Кадэ (1731— 1799) проводил перегонку ацетата калия с оксидом мышьяка(III). Сейчас уже сложно установить, что было целью того эксперимента. В результате же получилась жидкость с отвратительным чесночным запахом, самовоспламеняющаяся на воздухе. Поскольку это было явно не то, что хотел получить любознательный аптекарь, то исследовать жидкость он не стал.
Про загадочное соединение вспомнили только в следующем веке. Роберт Бунзен, изучая жидкость Кадэ, обнаружил в ней углерод, кислород, водород и мышьяк. В роли «крёстного отца» выступил Якоб Берцелиус, выделивший это вещество в чистом виде. Формула жидкости Кадэ — (CH3)2As—О—As(CH3)2, а название — окись какодила (от греч. «какос» — «дурной» и «одорос» — «запах»).
Если в неорганических соединениях свинец чаще всего двухвалентен, то для элементоорганических более характерна валентность свинца, равная четырём. Тетраэтилсвинец был известен ещё с 1853 г. Длительное время, начиная с 1923 г., он использовался как антидетонатор в моторном топливе (см. статью «Бесценное топливо»).
Это приводило к сильному загрязнению окружающей среды. Кроме того, соединения свинца быстро выводили из строя катализаторы очистки выхлопных газов от оксида углерода. В результате количество фильтров на выхлопной трубе стало резко увеличиваться, а сам автомобиль начал превращаться в химическую лабораторию в миниатюре. Дешевле оказалось получать более дорогой, но в то же время более качественный бензин, чем решать проблемы с очисткой от свинца продуктов сгорания этилированного бензина.
Широкое применение в самых разных областях получили и оловоорганические соединения. В основном они используются как стабилизаторы одного из самых распространённых пластиков — поливинилхлорида. Чистый поливинилхлорид начинает разлагаться и темнеть при 110 °С, тогда как его термическая переработка возможна только при 180 °С. Добавление производных диоктилстаннана типа (C8H17)2Sn(SCH2COOC8H17)2значительно повышает температуру разложения этого полимера, и его обработка становится гораздо легче.
Некоторые оловоорганические соединения довольно токсичны, в отличие от малотоксичных неорганических производных этого металла. Так, весьма ядовиты моно- и тетразамещённые станнаны RSnX3 и R4Sn, но особенно — тризамещённые R3SnX: они блокируют энергообмен в живой клетке. А вот механизм токсического действия дизамещённых станнанов пока не выяснен. Именно токсические свойства тризамещенных станнанов оказались наиболее востребованы. Производные трибутилолова используются как высокоэффективные дезинфицирующие средства.
Кремний и углерод — близкие родственники. Многие соединения кремния имеют углеродные аналоги, а сам он, как и углерод, может образовывать цепочки атомов. Неслучайно поэтому в научной фантастике встречаются рассуждения на тему «кремниевых» миров — биологических систем, в которых роль углерода в построении молекул играет кремний.
Однако вероятность существования кремниевых организмов даже в дальнем космосе крайне мала. Пока не удалось построить кремниевый аналог хоть сколько-нибудь сложной биологический молекулы. К концу XX в. получены соединения, содержащие кремниевые цепочки длиной до пяти атомов. И если гексаметилдисилан (CH3)3Si—Si(CH3).. достаточно устойчив, то уже производное трисилана (CH3)3Si—Si(CH3)2—Si(CH3)3легко окисляется на воздухе. А соединения, содержащие цепочки из четырёх или пяти атомов кремния, на воздухе самовоспламеняются. Синтезирован только один аналог алкенов — тетрамезитилдисилен; в нём атомы кремния со всех сторон «прикрыты» триметилбензольными (мезитиленовыми) кольцами.
Кремниевые аналоги алкинов и более сложных органических молекул получить пока не удалось.
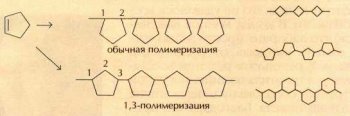
Во-вторых, подобные полимеры обладают исключительной термостойкостью. Полициклопентен плавится при 395 °С, полициклобутен — при 485 °С, а полициклогексен — при 600 °С, что сопоставимо с температурой размягчения оконного стекла.
Не много можно найти органических соединений, которые бы не разлагались при такой температуре.