Нитрид бора BN по структуре подобен углероду: в обоих веществах (в равных молярных количествах) содержится одинаковое число электронов. Как и углерод, нитрид бора существует в двух формах, построенных аналогично алмазу и графиту. При взаимодействии оксида бора с аммиаком в присутствии сажи при температуре порядка 2000 °С образуется нитрид бора со структурой графита: В2О3+3С+2NH3=2BN+3СО+3Н2. При высоких давлениях он переходит в алмазоподобную модификацию — боразон.
На основе нитрида бора созданы огнеупорные материалы, в том числе термостойкое волокно. Разные модификации нитрида бора используют как смазку для подшипников и как сверхтвёрдый абразивный материал — порошкообразное вещество, служащее для механической обработки металлов, сплавов, камней и т. п.
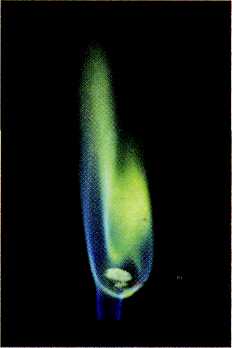
Обнаружить присутствие бора в веществе несложно: летучие соединения бора окрашивают пламя в зелёный цвет. В этом можно убедиться, внеся в пламя горелки несколько кристалликов борной кислоты.
Хотя элемент бор встречается в природе сравнительно редко (в земной коре его почти в 7 тыс. раз меньше, чем алюминия), главным образом в виде солей борной кислоты, бура — кристаллогидрат тетрабората натрия Na7B4O7•10Н2О — была известна уже в раннем Средневековье. В сочинениях арабских алхимиков говорится об использовании её в качестве плавня, а также для пайки драгоценных металлов. С Памира и с отрогов Гималаев буру доставляли караванами в Багдад.
Долгое время состав буры оставался неизвестным. Лишь в 1702 г. ученик Роберта Бойля Вильгельм Гомберг (1662—1715), прокаливая буру с железным купоросом, получил борную кислоту Н3ВО3, которую назвал успокоительной солью (sal sedativum) no будто бы производимому ею действию. Это вещество нашло широкое применение в медицине того времени. Спустя полвека было доказано, что бура является солью борной кислоты: она образуется при взаимодействии «успокоительной соли» с содой Na2CO3.